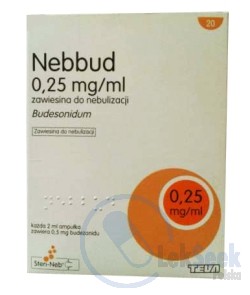
WskazaniaDawka 0,125 mg/ml. Budezonid w postaci zawiesiny do nebulizacji jest wskazany do stosowania u pacjentów dorosłych, młodzieży oraz u niemowląt i dzieci w wieku 6 m-cy i starszych. Astma. Budezonid w postaci zawiesiny do nebulizacji jest wskazany w leczeniu przewlekłej astmy oskrzelowej u pacjentów, u których stosowanie inhalatora ciśnieniowego lub inhalatora proszkowego jest niezadowalające lub niewłaściwe. Pseudokrup. Bardzo ciężkie zapalenie krtani - pseudokrup (laryngitis subglottica), w którym zalecana jest hospitalizacja. Dawka 0,25mg/ml; 0,5 mg/ml. Produkt w postaci zawiesiny do nebulizacji wskazany jest do stosowania: u pacjentów z astmą oskrzelową, u których stosowanie inhalatorów ciśnieniowych z dozownikiem lub inhalatorów proszkowych nie powoduje wystarczającego działania bądź jest niewskazane, u niemowląt i dzieci z pseudokrupem czyli ostrym zapaleniem krtani (laryngitis acuta), w leczeniu zaostrzenia przewlekłej obturacyjnej choroby płuc (POChP), w przypadku gdy stosowanie budezonidu w postaci zawiesiny do nebulizacji jest uzasadnione.DawkowanieDawka 0,25 mg/2 ml (0,125/ml). Astma. Dawkę leku należy przyjmować 2x/dobę. Stosowanie leku raz/dobę należy rozważyć u pacjentów ze stabilną astmą o lekkim lub umiarkowanym przebiegu. Dawka początkowa. Dawkę początkową należy dostosować do stopnia ciężkości choroby, a następnie do indywidualnych potrzeb pacjenta. Zalecane dawki wymieniono poniżej, ale zawsze należy stosować najmniejszą skuteczną dawkę. Dzieci w wieku 6 m-cy i starsze: 0,25-1 mg/dobę. U dzieci przyjmujących doustne steroidy jako leczenie podtrzymujące należy rozważyć zastosowanie większej dawki początkowej do 2,0 mg/dobę. Dorośli (w tym osoby w podeszłym wieku) i młodzież w wieku powyżej 12 lat: 0,5-2,0 mg/dobę. W bardzo ciężkich przypadkach dawkę można zwiększyć. Dawka podtrzymująca. Dawkę podtrzymującą należy dostosować do indywidualnych potrzeb pacjenta, biorąc pod uwagę nasilenie choroby oraz kliniczną odpowiedź pacjenta. Po uzyskaniu pożądanego działania klinicznego dawkę podtrzymującą należy zmniejszyć do najmniejszej dawki, zapewniającej skuteczną kontrolę objawów. Dzieci w wieku 6 miesięcy i starsze: 0,25-1,0 mg/dobę. Dorośli (w tym osoby w podeszłym wieku) i młodzież w wieku powyżej 12 lat: 0,5-2,0 mg/dobę. W bardzo ciężkich przypadkach dawkę można dodatkowo zwiększyć. Pseudokrup. Niemowlęta i dzieci: Zwykle stosowana dawka to 2 mg budezonidu podane w postaci nebulizacji. Można podać tę dawkę w całości lub podzielić ją na dwie i podać dwie dawki po 1 mg w odstępie 30 min. Ten sposób dawkowania może być powtarzany co 12 h, maks. do 36 h lub do uzyskania poprawy stanu klinicznego. Dzieci i młodzież. Nie określono bezpieczeństwa stosowania i skuteczności produktu leczniczego u niemowląt poniżej 6 m-cy. Dawka 0,5 mg/ml. Dawkę produktu należy ustalać indywidualnie dla każdego pacjenta. Dawkę należy zmniejszyć do najmniejszej dawki zapewniającej odpowiednią kontrolę astmy. Jeżeli zalecana dawka dobowa leku wynosi do 1 mg, produkt można stosować raz/dobę. Produkt można stosować raz/dobę u pacjentów nie leczonych dotychczas glikokortykosteroidami oraz u pacjentów z dobrze kontrolowanymi objawami choroby za pomocą wziewnych glikokortykosteroidów. Stosowany raz/dobę można podawać rano lub wieczorem. Jeżeli nastąpi zaostrzenie objawów choroby, należy zwiększyć dawkę dobową produktu. Podczas stosowania dawki dobowej większej niż 1 mg, produkt należy podawać 2x/dobę. W celu zminimalizowania ryzyka zakażenia grzybiczego jamy ustnej i gardła, pacjent powinien po inhalacji wypłukać usta wodą. Ważne jest, aby poinformować pacjenta lub opiekuna o konieczności umycia wodą skóry twarzy po użyciu maski na twarz w celu zapobieżenia podrażnieniom skóry twarzy. Dawka początkowa. Podczas rozpoczynania leczenia, w okresach zaostrzenia astmy oraz podczas zmniejszania dawki lub odstawiania glikokortykosteroidów doustnych zalecana dawka produktu wynosi: Dorośli (w tym pacjenci w podeszłym wieku) i młodzież w wieku powyżej 12 lat: 1-2 mg/dobę. W bardzo ciężkich przypadkach dawkę można zwiększyć. Dzieci w wieku od 6 m-cy do 12 lat: 0,25-0,5 mg/dobę. U dzieci, które zażywają doustnie glikokortykosteroidy, można w razie konieczności zwiększyć dawkę dobową do 1 mg. U małych dzieci, które nie mogą wdychać produktu przez ustnik, produkt powinien być podawany przez maskę twarzową. Dawka podtrzymująca. Dawkę podtrzymującą należy dostosować do potrzeb danego pacjenta. Po osiągnięciu działania leczniczego należy zmniejszyć dawkę podtrzymującą do najmniejszej dawki, która zapewnia odpowiednią kontrolę astmy. Dorośli (w tym pacjenci w podeszłym wieku) i młodzież w wieku powyżej 12 lat: całkowita dawka dobowa wynosi od 0,5 do 4 mg. Dzieci w wieku od 6 m-cy do 12 lat: całkowita dawka dobowa wynosi 0,25-2 mg/dobę. Poprawa stanu klinicznego po zastosowaniu produktu może nastąpić w ciągu kilku godz. od rozpoczęcia leczenia. Pełne działanie lecznicze uzyskuje się po kilku tyg. od rozpoczęcia leczenia. Pacjenci przyjmujący doustne glikokortykosteroidy: produkt może umożliwić zastąpienie lub zmniejszenie dawki doustnych glikokortykosteroidów zapewniając jednoczesne utrzymanie działania leczniczego. Więcej informacji na temat odstawiania doustnych glikokortykosteroidów, patrz ChPL. Astma. Po uzyskaniu właściwej kontroli astmy, stosowanie budezonidu w postaci zawiesiny do nebulizacji pozwala na zastąpienie lub znaczące zmniejszenie dawki doustnych glikokortykosteroidów. Podczas zmiany leczenia z doustnych glikokortykosteroidów na leczenie budezonidem w postaci zawiesiny do nebulizacji pacjent powinien być we względnie stabilnym stanie. Zaleca się stosowanie przez 10 dni dużych dawek budezonidu w postaci zawiesiny do nebulizacji w skojarzeniu z wcześniej stosowanym glikokortykosteroidem doustnym w niezmienionej dawce. Następnie dawka doustnego glikokortykosteroidu powinna być stopniowo zmniejszana (np. mniej więcej o 2,5 mg prednizolonu lub równoważną dawkę innego glikokortykosteroidu na miesiąc) do możliwie najmniejszego poziomu zapewniającego kontrolę objawów choroby. Często stosowanie doustnych glikokortykosteroidów można całkowicie zastąpić budezonidem w postaci zawiesiny do nebulizacji. Dalsze informacje dotyczące przerwania stosowania glikokortykosteroidów, patrz ChPL. Pseudokrup. Zwykle stosowana dawka u niemowląt i dzieci z pseudokrupem to 2 mg budezonidu podane w postaci nebulizacji. Można podać tę dawkę w całości lub podzielić ją na dwie i podać dwie dawki po 1 mg w odstępie 30 min. Ten sposób dawkowania może być powtarzany co 12 h, maks. do 36 h lub do uzyskania poprawy stanu klinicznego. Zaostrzenia POChP. Na podstawie ograniczonych danych z badań klinicznych zalecana dawka produktu, zawiesina do nebulizacji wynosi od 4-8 mg/dobę, podzielona na 2-4 podań. Leczenie należy prowadzić aż do uzyskania poprawy stanu klinicznego, przy czym nie zaleca się leczenia dłuższego niż przez 10 dni. Podział dawek i mieszalność. Produkt w postaci zawiesiny do nebulizacji może być mieszany z 0,9% roztworem chlorku sodu lub z innymi roztworami do nebulizacji terbutaliny, salbutamolu, fenoterolu, acetylocysteiny, kromoglikanu disodowego bądź bromku ipratropiowego. Całkowita objętość zawiesiny znajdująca się w plastikowym pojemniku (amp.) może być dzielona w celu uzyskania odpowiedniej dawki. Amp. jest oznakowana poziomą linią przerywaną. Po odwróceniu amp. zamknięciem do dołu linia ta oznacza objętość 1 ml. Jeśli ma być użyty tylko 1 ml, należy usunąć płyn znajdujący się nad linią wskaźnikową. Otwarty pojemnik plastikowy należy zawsze przechowywać w folii laminowanej, w oryginalnym opakowaniu. Zawartość otwartej amp. nadaje się do użycia w ciągu 12 h. Zalecane dawkowanie, szczegóły patrz ChPL.UwagiWyłącznie do podawania wziewnego. Należy zachować ostrożność podczas przygotowywania i podawania produktu leczniczego. Lek przeznaczony jest do podawania wziewnego. Nie należy używać ampułek częściowo zużytych, otwartych lub uszkodzonych. Lek należy podawać za pomocą odpowiedniego nebulizatora o konstrukcji zapewniającej wytwarzanie cząstek o właściwej wielkości pozwalającej małym kroplom na przejście do płuc. Zazwyczaj będą miały one DV(50) <3µm oraz DV(90) <6µm. Produkt leczniczy należy podawać za pomocą odpowiednich nebulizatorów. Nebulizatory ultradźwiękowe nie nadają się do podawania produktu. Dawka budezonidu dostarczonego pacjentowi różni się w zależności od zastosowanego zestawu do nebulizacji. Czas nebulizacji oraz dostarczana dawka leku zależą od prędkości nebulizacji, objętości komory nebulizatora oraz od jej napełnienia. Lek należy podawać za pomocą nebulizatora dyszowego wyposażonego w ustnik lub odpowiednią maskę na twarz. Nebulizator powinien być podłączony do kompresora o odpowiednim przepływie powietrza (6-8 l/min), a objętość napełnienia powinna wynosić 2-4 ml. Należy poinstruować pacjentów w zakresie prawidłowego stosowania produktu. Dzieci oraz ich opiekunów należy zachęcić oraz przeszkolić do stosowania raczej ustnika niż maski na twarz. Instrukcja stosowania produktu: przygotować nebulizator do użycia zgodnie z zaleceniami producenta, oddzielić ampułkę z oznaczonego paska przez przekręcenie i pociągnięcie, delikatnie wstrząsnąć ampułką. Trzymając ampułkę pionowo do góry odkręcić zamknięcie. Ampułka oznaczona jest linią przerywaną wskazującą objętość 1 ml, jeżeli pojemnik odwróci się do góry dnem. Jeżeli ma być użyta objętość tylko 1 ml należy opróżnić zawartość pojemnika do poziomu linii wskaźnikowej. Otwarty pojemnik plastikowy należy przechowywać w folii, w oryginalnym opakowaniu.Zawartość plastikowego pojemnika jednostkowego nadaje się do użycia w ciągu 12 h od jego otwarcia. Wycisnąć odpowiednią ilość zawiesiny z ampułki do komory nebulizatora. Użyć nebulizatora zgodnie z zaleceniami producenta. Komorę nebulizatora umyć i wysuszyć. Komorę nebulizatora oraz ustnik lub maskę na twarz należy umyć w gorącej wodzie z dodatkiem łagodnego detergentu. Starannie wypłukać i wysuszyć podłączając komorę nebulizatora do wlotu sprężonego powietrza lub kompresora. Pacjentów należy poinstruować, aby po zakończeniu inhalacji zalecanej dawki przepłukiwali jamę ustną wodą w celu zmniejszenia ryzyka kandydozy jamy ustnej i gardła. Pacjentów stosujących maskę na twarz należy poinstruować, aby po zakończeniu inhalacji myli twarz wodą w celu uniknięcia podrażnień. Ważne! Pacjentów należy poinstruować, aby: uważnie przeczytali zalecenia dotyczące stosowania znajdujące się w Ulotce dla Pacjenta dołączonej do każdego opakowania produktu do nebulizacji; przygotowali nebulizator do użycia zgodnie z zaleceniami producenta; przepłukiwali jamę ustną wodą po zakończeniu inhalacji zalecanej dawki w celu zmniejszenia ryzyka wystąpienia pleśniawek jamy ustnej i gardła (kandydozy); w przypadku stosowania maski na twarz, myli twarz po zakończeniu inhalacji w celu uniknięcia podrażnień. Pacjentów należy poinformować, że nebulizatory ultradźwiękowe nie są odpowiednie do podawania budezonidu w postaci zawiesiny do nebulizacji i nie są do tego zalecane. PrzeciwwskazaniaNadwrażliwość na substancję czynną lub na którąkolwiek substancję pomocniczą.Ostrzeżenia specjalne / Środki ostrożnościLek nie jest wskazany do stosowania w leczeniu ostrej duszności oraz stanu astmatycznego. W takich przypadkach należy stosować krótkodziałające b2-mimetyki i inne leki rozszerzające oskrzela. Szczególną ostrożność należy zachować w przypadku pacjentów z gruźlicą płuc i zakażeniami wirusowymi dróg oddechowych. Lek można stosować u tych pacjentów tylko wtedy, gdy schorzenia te są odpowiednio leczone. Działanie terapeutyczne występuje zazwyczaj w ciągu 10 dni od rozpoczęcia leczenia. U pacjentów z obfitą wydzieliną oskrzelową można zalecić początkowo krótkotrwałe leczenie skojarzone (przez około 2 tyg.) doustnymi kortykosteroidami. Po zakończeniu terapii doustnej leczenie produktem w postaci wziewnej w monoterapii powinno być wystarczające. Zmiana leczenia z doustnych kortykosteroidów na kortykosteroidy wziewne oraz dalsze prowadzenie terapii wymaga, w takich przypadkach, zachowania szczególnej ostrożności. Przystąpienie do zmiany leczenia z doustnych kortykosteroidów na leczenie budezonidem w postaci wziewnej może nastąpić wówczas, gdy stan pacjenta jest względnie stabilny. Produkt należy podawać jednocześnie ze stosowanymi dotychczas steroidami doustnymi przez około 10 dni. Następnie dawkę tych leków należy stopniowo zmniejszać (przykładowo o 2,5 mg prednizolonu lub równoważną dawkę odpowiednika na m-ąc), aż do osiągnięcia min. skutecznego poziomu. W wielu przypadkach możliwe jest całkowite zastąpienie doustnych kortykosteroidów produktem. Pacjenci, u których po przejściu na leczenie kortykosteroidami wziewnymi wystąpią zaburzenia czynności kory nadnerczy, mogą wymagać leczenia uzupełniającego kortykosteroidami ogólnoustrojowymi w okresach stresu związanego np. z zabiegami chirurgicznymi, zakażeniem lub nasileniem ataków astmy. Dotyczy to również pacjentów leczonych długotrwale dużymi dawkami kortykosteroidów wziewnych, u których także mogą wystąpić zaburzenia czynności nadnerczy skutkujące klinicznie istotną niewydolnością kory nadnerczy. Pacjenci tacy mogą również wymagać ogólnoustrojowego leczenia kortykosteroidami w okresach ciężkich sytuacji stresowych. Zazwyczaj ogólnoustrojowe działanie steroidów zmniejsza się podczas zmiany z leczenia doustnego na leczenie produktem, powodując objawy alergiczne lub artretyczne takie, jak zapalenie błony śluzowej nosa, wyprysk oraz ból mięśni i stawów. Należy wówczas zastosować leczenie właściwe dla tych objawów. W rzadkich przypadkach, na niewystarczającą aktywność glikokortykosteroidową mogą wskazywać takie objawy, jak zmęczenie, ból głowy, nudności i wymioty. W tych przypadkach jest niekiedy konieczne okresowe zwiększenie dawki doustnych glikokortykosteroidów. Podobnie, jak w przypadku innych leków wziewnych, może wystąpić paradoksalny skurcz oskrzeli z nasileniem świstów bezpośrednio po podaniu dawki. Jeśli wystąpi ciężka reakcja, należy ponownie ocenić leczenie i w razie konieczności rozpocząć leczenie alternatywne. Jeśli pomimo dobrze kontrolowanego leczenia u pacjenta wystąpi ostry napad duszności, należy zastosować szybko działający, wziewny lek rozszerzający oskrzela i rozważyć ponowną ocenę leczenia. Jeśli pomimo zastosowania maks. dawek kortykosteroidów wziewnych nie udaje się w odpowiednim stopniu opanować objawów astmy, może być konieczne zastosowanie u pacjenta krótkotrwałego leczenia kortykosteroidami działającymi ogólnoustrojowo. W takich przypadkach konieczne jest kontynuowanie leczenia kortykosteroidami wziewnymi w skojarzeniu z leczeniem ogólnoustrojowym. Możliwe jest wystąpienie ogólnoustrojowych działań kortykosteroidów wziewnych, szczególnie w długotrwałych okresach leczenia dużymi dawkami leku. Wystąpienie takich działań jest dużo mniej prawdopodobne niż w przypadku leczenia kortykosteroidami doustnymi. Możliwe działania ogólnoustrojowe to zespół Cushinga, wygląd jak w zespole Cushinga, zahamowanie czynności nadnerczy, opóźnienie wzrostu u dzieci i młodzieży, zmniejszenie gęstości mineralnej kości, zaćma, jaskra a rzadziej wachlarz skutków psychologicznych i behawioralnych w tym nadaktywność psychoruchowa, zaburzenia snu, lęk, depresja lub agresja (szczególnie u dzieci).Dlatego też ważne jest, aby zwiększać dawkę kortykosteroidu wziewnego do najmniejszej skutecznej dawki utrzymującej kontrolę objawów astmy. Zaleca się regularne kontrolowanie wzrostu u dzieci długotrwale leczonych kortykosteroidami wziewnymi. W przypadku opóźnienia wzrostu należy dokonać oceny leczenia pod kątem możliwości zmniejszenia dawki kortykosteroidu wziewnego do najniższej dawki skutecznej utrzymującej kontrolę objawów astmy. Ponadto należy rozważyć skierowanie pacjenta do lekarza pediatry specjalizującego się w chorobach dróg oddechowych. Lek nie jest wskazany do leczenia ostrych napadów astmy, w których wymagane jest zastosowanie krótkodziałającego leku wziewnego rozszerzającego oskrzela. W przypadku, gdy krótkodziałający lek rozszerzający oskrzela okaże się nieskuteczny lub pacjent będzie wymagał większej niż zwykle liczby inhalacji, należy skonsultować się z lekarzem. W takiej sytuacji należy rozważyć wzmocnienie ich stałego leczenia np. poprzez zwiększenie dawek budezonidu wziewnego, dodanie długodziałającego b-agonisty lub zastosowanie kursu leczenia doustnym glikokortykosteroidem. Zaburzenia czynności wątroby mogą prowadzić do spowolnienia wydalania glikokortykosteroidów. Jednakże klirens osoczowy po podaniu dożylnej dawki budezonidu pacjentom z marskością wątroby i osobom zdrowym był podobny. Po podaniu doustnym obserwowano wzrost dostępności ogólnoustrojowej budezonidu przy zaburzonej czynności wątroby w wyniku zmniejszenia metabolizmu pierwszego przejścia. Kliniczne znaczenie tej obserwacji dla przebiegu leczenia produktem nie jest znane, ponieważ brak danych dla budezonidu wziewnego, niemniej jednak można spodziewać się wzrostu stężeń w osoczu i zwiększenia ryzyka niepożądanych działań ogólnoustrojowych. Badania in vivo wykazały, że doustne podawanie ketokonazolu i itrakonazolu (znanych inhibitorów działania izoenzymu CYP3A4 w wątrobie i błonie śluzowej jelit) powoduje zwiększenie ogólnoustrojowej ekspozycji na budezonid. Należy unikać jednoczesnego podawania ketokonazolu, itrakonazolu oraz innych silnych inhibitorów CYP3A4. Jeśli nie jest to możliwe przerwa pomiędzy podaniem wchodzących w interakcje leków powinna być jak najdłuższa. Można również rozważyć zmniejszenie dawki budezonidu. W celu ograniczenia ryzyka kandydozy jamy ustnej oraz chrypki należy poinstruować pacjentów, aby: po każdej inhalacji płukali jamę ustną wodą w celu zmniejszenia ryzyka wystąpienia grzybicy jamy ustnej i gardła; po każdym użyciu maski na twarz przemywali twarz wodą w celu uniknięcia podrażnienia skóry. Zakażenia grzybicze jamy ustnej można szybko wyleczyć stosując leki przeciwgrzybicze o działaniu miejscowym, bez konieczności przerywania leczenia produktem. Produkt nie ma wpływu lub wywiera nieistotny wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn.InterakcjeBudezonid jest metabolizowany głównie przez izoenzym CYP3A4. W związku z tym inhibitory tego enzymu np. ketokonazol i itrakonazol, mogą zwiększać ekspozycję ogólnoustrojową na budezonid. Inne silne inhibitory CYP3A4 takie, jak erytromycyna, klarytromycyna, rytonawir i sakwinawir mogą również znacząco zwiększać stężenie budezonidu w osoczu. Jednoczesne podawanie cymetydyny może prowadzić do nieznacznego zwiększenia stężenia budezonidu w osoczu, które jest zazwyczaj nieistotne klinicznie. Jednoczesne stosowanie budezonidu ze steroidami o działaniu ogólnoustrojowym lub podawanymi donosowo prowadzi do addytywnego działania hamującego czynność nadnerczy.Ciąża i laktacjaStosowanie budezonidu w okresie ciąży jest możliwe jedynie wówczas, gdy korzyści dla matki przewyższają ryzyko dla płodu. Rozważając leczenie, należy preferować zastosowanie glikokortykosteroidów wziewnych w porównaniu z glikokortykosteroidami doustnymi, z powodu ich słabszego działania ogólnoustrojowego w dawkach wymaganych do uzyskania podobnej odpowiedzi płucnej. Noworodki urodzone przez matki leczone budezonidem w okresie ciąży należy monitorować, czy nie występuje u nich niedoczynność kory nadnerczy. Badania na zwierzętach wykazały, że glikokortykosteroidy mogą zwiększać możliwość zniekształceń płodów. Jednakże nie dotyczy to ludzi, jeżeli budezonid jest stosowany w zalecanych dawkach, lecz leczenie wziewnym budezonidem należy regularnie oceniać i stosować najmniejszą skuteczną dawkę. Dane dotyczące przebiegu ciąży u 2000 kobiet wskazują, że nie zwiększa się ryzyko teratogenności związane ze stosowaniem wziewnego budezonidu. Budezonid przenika do mleka matki. Jednakże w przypadku stosowania budezonidu w dawkach leczniczych nie przewiduje się żadnego wpływu leku na karmione niemowlę. Lek można stosować w okresie karmienia piersią.Działania niepożądaneZakażenia i zarażenia pasożytnicze: (często) kandydoza jamy ustnej i gardła. Zaburzenia układu immunologicznego: (rzadko) natychmiastowe i opóźnione reakcje nadwrażliwości. Zaburzenia endokrynologiczne: (bardzo rzadko) zahamowanie czynności kory nadnerczy. Zaburzenia psychiczne: (nieznana) nadpobudliwość psychoruchowa, zaburzenia snu, lęk, depresja, agresja, zmiany w zachowaniu (głównie u dzieci). Zaburzenia oka: (bardzo rzadko) zaćma, jaskra. Zaburzenia układu oddechowego, klatki piersiowej i śródpiersia: (często) chrypka, kaszel; (rzadko) paradoksalny skurcz oskrzeli. Zaburzenia żołądka i jelit: (często) podrażnienie błony śluzowej jamy ustnej, trudności w przełykaniu. Zaburzenia skóry i tkanki podskórnej: (rzadko) podrażnienia skóry twarzy, wysypka, zapalenie skóry, pokrzywka, świąd, rumień, siniaczenie, obrzęk naczynioruchowy. Zaburzenia mięśniowo-szkieletowe i tkanki łącznej: (bardzo rzadko) opóźnienie wzrostu u dzieci i młodzieży, zmniejszona gęstość mineralna kości. Zakażenia grzybicze jamy ustnej i gardła spowodowane są depozycją leku. Ryzyko zakażeń można zmniejszyć, gdy pacjent wykonuje inhalacje produktem przed posiłkami i płucze jamę ustną po inhalacji. W większości przypadków kandydoza odpowiada na leczenie miejscowe i nie wymaga odstawienia budezonidu. Aby zapobiec występowaniu kaszlu można wykonać doraźną inhalację b2-mimetyku 5-10 min. przed podaniem produktu. Zdolność przystosowania do sytuacji stresowych może być zaburzona. PrzedawkowanieOstre przedawkowanie budezonidu nie powinno stanowić problemu klinicznego. Budezonid stosowany długotrwale w dużych dawkach może powodować zahamowanie czynności nadnerczy. Ostre przedawkowanie: nie ma konieczności podejmowania szczególnych działań doraźnych. Należy kontynuować leczenie budezonidem w najmniejszej skutecznej dawce podtrzymującej. Prawidłowa czynność kory nadnerczy powraca samoistnie w ciągu kilku dni. Przedawkowanie przewlekłe: należy postępować tak, jak w przypadku pacjentów leczonych wcześniej steroidami. Należy zastosować odpowiednią dawkę podtrzymującą steroidu o działaniu ogólnoustrojowym np. prednizolonu. Kiedy stan pacjenta ustabilizuje się, pacjent powinien kontynuować leczenie budezonidem wziewnym w zalecanej dawce.DziałanieBudezonid jest glikokortykosteroidem wykazującym silne miejscowe działanie przeciwzapalne, o mniejszej liczbie i nasileniu działań niepożądanych w porównaniu do kortykosteroidów doustnych. Dokładny mechanizm działania glikokortykosteroidów w leczeniu astmy nie jest w pełni poznany. Prawdopodobnie ważną rolę odgrywają reakcje przeciwzapalne polegające na zahamowaniu uwalniania mediatorów zapalenia i zahamowaniu odpowiedzi immunologicznej zależnej od cytokin. Badanie kliniczne, z udziałem pacjentów z astmą porównujące działanie budezonidu wziewnego i doustnego w dawkach zapewniających zbliżoną biodostępność ogólnoustrojową, wykazały statystycznie istotną skuteczność budezonidu wziewnego, ale nie doustnego. Dlatego też, działanie terapeutyczne standardowych dawek wziewnego budezonidu można w większości wytłumaczyć bezpośrednim jego działaniem na drogi oddechowe. W testach prowokacyjnych wykazano, że wcześniejsze leczenie budezonidem przez 4 tyg. powoduje mniejsze zwężenie oskrzeli we wczesnych, jak również późnych reakcjach astmatycznych.Skład1 amp. o pojemności 2 ml zawiera 0,125 mg, 0,25 mg lub 0,5 mg budezonidu.











 Grejpfrut
Grejpfrut Ciąża - trymestr 1 - Kategoria B
Ciąża - trymestr 1 - Kategoria B Ciąża - trymestr 2 - Kategoria B
Ciąża - trymestr 2 - Kategoria B Ciąża - trymestr 3 - Kategoria B
Ciąża - trymestr 3 - Kategoria B Wykaz B
Wykaz B Papierosy
Papierosy



Komentarze
[0 z 0]